相信了解过一些化学研究的同学们都对“过柱子”这个词并不陌生。所谓过柱子,其实是色谱法中的一种——柱层析。正好最近分析化学课程中学了相关知识,那就来给大家分类介绍一下色谱法,权当期末复习(
先放一个百度百科对于色谱法的总定义:“色谱法利用不同物质在不同相态的选择性分配,以流动相对固定相中的混合物进行洗脱,混合物中不同的物质会以不同的速度沿固定相移动,最终达到分离的效果。”简而言之,可以把流动相理解为动力来源,固定相理解为阻力来源,由于物质性质不同,在固定相的影响下通过柱子的时间不同,就能挨个分离检测了。
其实色谱的分类方法有很多种,例如按照流动相和固定相的物态划分:气固色谱法,气液色谱法,液固色谱法,液液色谱法 。这里把流动相的物态放在名字的前面,固定相放在后面。正常情况下固态物质是不可能作为流动相的,气态物质也不会作为固定相,所以也不可能出现“固~色谱”“~气色谱”。
也有按照固定相形式分类的,例如纸色谱(高中生物分离菠菜叶色素),薄层色谱,柱色谱。
本文要用的分类方法,是按照色谱法的原理进行分类介绍,方便大家对于色谱法有更深的了解。
1 吸附色谱法 Adsorption Chromatography:
吸附色谱法通常采用固态固定相,利用固态吸附剂对于通过物质不同程度的吸附来达到分离的效果。这里的吸附作用大多指分子间作用力,例如疏水作用力,芳环相互作用,较强的也会有一定的氢键作用,因此常常是和吸附剂及分析物质的极性密切相关的。极性相似的物质之间相互作用力就更强,所以与固定相极性越相似的物质,被吸附的时间更长,通过柱子的时间也就更长。通常情况下,流动相的极性和固定相是相反的,所以是最快通过的物质。
根据固定相极性的大小,通常把色谱分为正相色谱(固定相高极性,流动相低极性或者无极性);反相色谱(固定相低极性或者无极性,流动相高极性)。需要注意的是,此处的正反相色谱尽依靠固定相和流动相的极性分类,和分离原理无关,所以正反相色谱不一定是吸附色谱或者下面要说的分配色谱。
在实验课上,我们又做了一次菠菜叶色素的分类,但是这次用的是柱色谱。我们用的固定相是C18 结合在硅胶球上,具体结构如下:C18由于基本上全是烃基碳链,基本上是无极性的,所以对极性低的色素吸附能力较强,属于反相色谱。
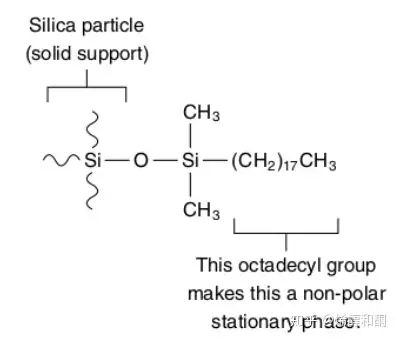
经过色谱分离后,我做出来的谱图如下:
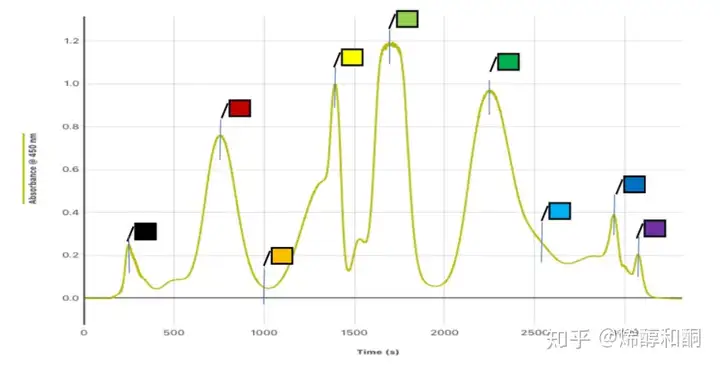
其中每一个峰就代表一个(或者多个极性相近的)色素。信号检测是测的对于450nm波长光的吸收。横轴是时间轴,越靠前峰代表极性越强的色素,最前面的峰是流动相(水,乙腈,乙酸乙酯混合物)
2 分配色谱法 Partitioning Chromatography:
说分配色谱法就不得不提大家的一个高中化学小实验:萃取。利用溶质在两种不混溶的溶剂中溶解度不同,将溶质集中到溶解度高的溶剂中。而分配色谱法就像是在通过柱子的过程中不断进行微观尺度上的萃取。在SP中溶解度高的溶质就会在SP中停留更长的时间,进而更迟通过柱子并被检测到。
分配色谱法和吸附色谱法的主要区别在于固定相的物态,如果固定相是固态,就不存在什么溶解度的问题,只能通过吸附作用结合分析物。相反的,分配色谱的固定相的液态。肯定有人会奇怪,这个液体你怎么固定,它不流下来吗?其实分配色谱中液态的固定相是结合在固态物质上的,有可能是管壁,也有可能是填充的小颗粒。
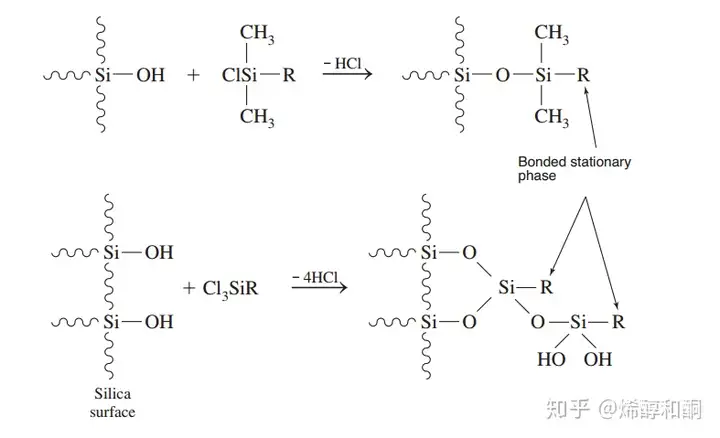
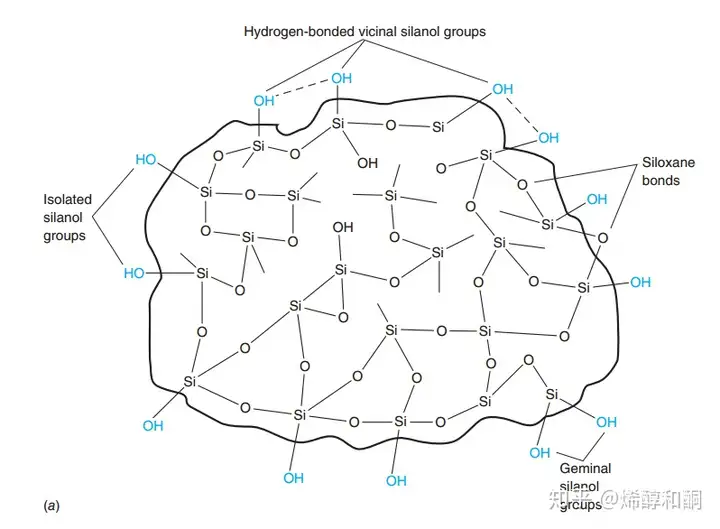
3 离子交换法 Ion-exchange Chromatography:
离子交换色谱通常有着带电荷的固定相,通常是带有阳离子或者阴离子的树脂等有机物。这些带电荷的基团和一些电性想法的离子相结合,不同离子和固定相基底的亲和性不同,进而做到离子的分离和交换。分析物在通过柱子的时候在不断进行着离子结合与分离的平衡,最终结合能力更强的离子将会与固定相结合,结合能力弱的离子被洗脱下来。通常是电荷更高,水合半径更小,极化能力越强的离子结合能力更强。我们用离子选择性常数(ion selectivity)来表示结合能力,越高结合能力越强。
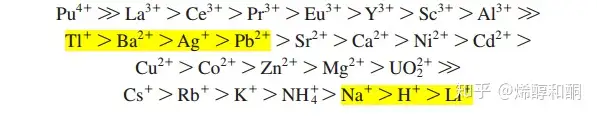
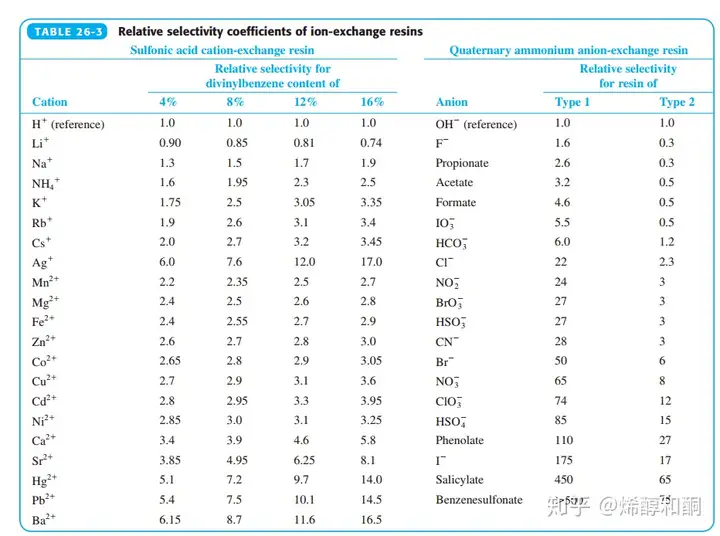
我们通常把离子交换色谱分为阳离子交换,阴离子交换和同时交换,下面分别举例介绍:[SP]表示固定相的结合基团
阳离子交换:固定的有机阴离子,例如磺酸基、羧基等。原本的阴离子基团上会附着阳离子,被通过柱子的亲和性更强的阳离子取代,原先附着的阳离子被洗脱。
([SP]Li+ + KCl-->[SP]K+ + LiCl)
阴离子交换:固定的有机样离子,例如季铵盐。原本的阳离子基团上会附着阴离子,被通过柱子的亲和性更强的阴离子取代,原先附着的阳离子被洗脱。 ([SP]OH- + KI-->[SP]I- + KOH)
同时交换阴阳离子:用可成内盐的两性有机物作为基底,同时结合阴阳离子,相当于二合一的柱子。([SP]Na+ and [SP]Cl- + LiI and KF-->NaF + LiCl + [SP]K+ and [SP]I-)
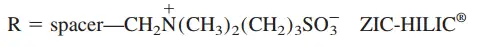
我们做离子交换色谱通常有两种目的,一是替换现有分析物中的阳/阴离子为另一种同电性离子。这样只需要替换的目的离子亲和力低于原离子,过一下柱子就能得到目标产物。也可能是需要分离出分析物中的某个离子,这样就需要将分析物中的离子先通过离子交换固定到柱子上,与有机的带电基团结合,然后再进行洗脱。离子的洗脱通常通过调节pH并流过大量洗脱液,拖动平衡,洗下目标离子。
4 尺寸排阻法 Size Exclusion Chromatography:
顾名思义,尺寸排阻法的核心就是利用分子尺寸的不同对分子进行分离。这种方法使用的固定相多为含有很多小孔的凝胶,这些小孔的大小不一,对于能通过的分子尺度就有不同程度的筛选。在尺寸排除色谱中,如果一个分子足够大,那它就不会通过任何小孔,而只能通过固定相之间的空隙,走最短的路程流出色谱柱,成为最先出现的峰。而极小的分子,还有流动相,都可以通过固定相凝胶所含的全部小孔,使其在流出色谱柱前走过了一条最为曲折的线路,显现出最后的峰。
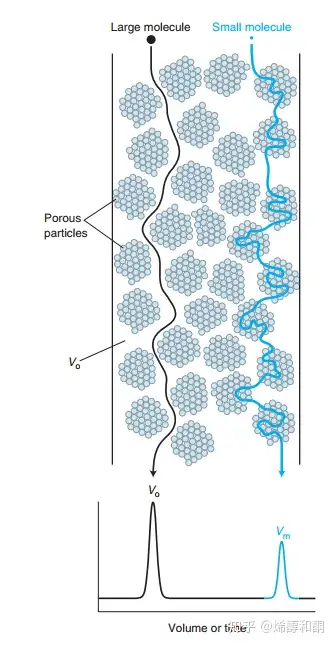
对于这种色谱的定量分析也非常有意思。由于流动相的流速是固定的,我们将出峰时间和物质通过的体积可以做一个线性对应。首先将色谱柱中除去固定相的所有体积称为总体积Vt。在Vt中,对分子大小无筛选作用的填充空隙,称为Vo。剩下的固定相小孔所占据的体积,称为Vm。Vm+Vo=Vt。一个分子在通过色谱柱时,将会经过所有的Vo;而由于尺寸限制,则只会经过部分可通过的Vm。如果将一个分子经过的真正体积称为Vr,我们可以定义出K:
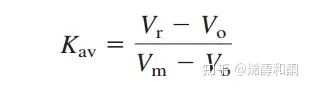
对于足够大的分子,K=0,对于无孔不入的小分子和流动相,K=1。通常情况下,K在0~1之间,但是如果分析物除了通过固定相的空隙和小孔以外,还和固定相产生了一定的吸附作用,进一步增长通过的时间,就可能出现K大于1的情况。
5 亲和色谱法 Affinity Chromatography:
亲和色谱法通常是色谱法中可以将选择性做到最高的一种,对于单一物质的严格筛选非常实用。在很多生物实验中,亲和色谱法利用的是酶和底物,或者抗体抗原的特异性结合。将这种特异性结合的一方作为固定相,从而在混合物中分离纯化出另一方。在我们的实验课上,我们使用的固定相是Ni-NTA琼脂凝胶,用来分离基因编译大肠杆菌合成的带有单一组氨酸残基区域的蛋白质,利用的是连续的组氨酸残基对镍原子的螯合结合。
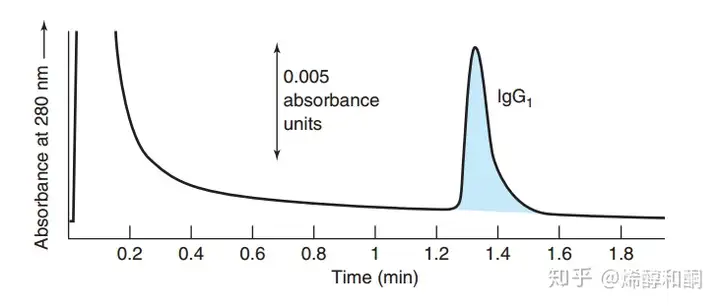
对于亲和色谱还有一个很有意思的部分就是洗脱,即目标产物和固定相结合后收获产物的步骤。首先我们通常会用一定量的清洗液进一步纯化分析柱中的物质,保证其中只剩下结合在固定相上的目标产物。接下来会用特殊的洗脱液解开目标产物和固定相之间的结合,通常的做法有改变pH、取代等。例如我们所做的对于上述蛋白的洗脱,是用含有较高浓度咪唑的缓冲溶液,替换掉连续组氨酸残基对于镍原子的螯合。随着咪唑对蛋白的取代,蛋白就会随之洗脱液流出分析柱。
总结:
本文按照不同原理,对于各种色谱方法进行了简要的介绍,方便大家再今后接触到的时候,至少对于实验在干什么有个基本的概念。色谱法的理论和具体运用远比文章中所展现的要纷繁复杂的多,有兴趣可以进一步深入了解。
参考文献:(分析化学课的教科书)
(1) Harris, D. C. Quantitive Chemical Analysis, ninth edit.; 2016.